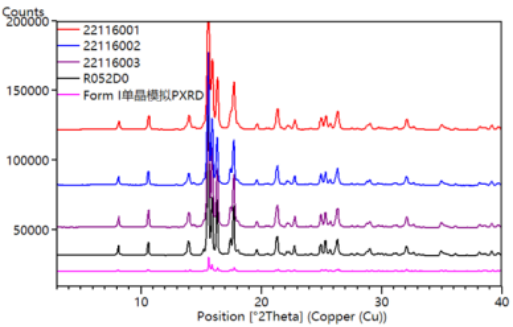
化合物的多晶型现象如同分子排列的 “百变密码”,不同晶型的药物在溶解度、溶出速率、稳定性乃至生物利用度上都可能存在显著差异。原料药和制剂中的杂质晶型是否需要研究?晶型质量控制该如何科学决策?这些问题都与晶型定性紧密相关。无论是从保障药物疗效与安全性的角度,还是从满足药品质量标准的要求出发,精准的晶型定性都是解开药物质量奥秘的重要钥匙。
化合物多晶型现象与研究必要性
化合物的多晶型现象是指同一种化合物在不同条件下能够形成两种或两种以上的晶体结构。这种现象的产生源于分子在晶格中排列方式、构象或结晶水 / 溶剂分子存在形式的差异。以某创新药晶型筛选为例,根据化合物特性设计的全面多晶型筛选试验共得到了14种新晶型。对于原料药和制剂而言,杂质晶型的研究并非可有可无。杂质晶型可能影响主药的稳定性,甚至改变药物的释放行为,从而对药品质量和安全性产生潜在威胁。因此,开展杂质晶型研究,通过晶型定性准确识别和控制杂质晶型,是确保药品质量均一性和有效性的必要举措 。
晶型质量控制的科学决策
晶型质量控制的决策需要综合多方面因素考量。首先要评估晶型对药物关键质量属性的影响程度,如果某种晶型会显著影响药物的溶出速率或稳定性,那么对其进行严格控制就至关重要。其次,需结合生产工艺的可行性和重现性,判断在实际生产过程中能否稳定获得目标晶型并有效控制杂质晶型。此外,法规要求也是重要的决策依据,监管部门对于一些关键药物的晶型控制往往有着明确规定。
在决策是否将晶型控制引入质量标准时,要权衡风险与收益。对于创新药,在研发初期可能只需对晶型进行初步定性研究,但随着研究的深入和临床数据的积累,若发现晶型对药物疗效影响显著,则应及时将晶型控制指标纳入质量标准。而对于仿制药,需确保其晶型与原研药一致,晶型定性研究更是必不可少,以保证药品的一致性评价顺利通过。
晶型定性分析服务内容
1、原料药及制剂晶型鉴别:晶型一致性分析、混晶/溶剂化物鉴别
原料药的不同晶型具有不同的物理和化学性质,原料药的不同晶型可具有不同的物理和化学性质,可能对原料药及制剂的稳定性、制剂的生产工艺、溶出度及生物利用度等产生影响,确认原料药的晶型可以保证药物的安全性、有效性和质量可控性。
2、原料药制剂中API晶型分析方法开发与验证:根据药典分析方法指导原则进行验证
在药物研发中,晶型分析方法是原料药及制剂开发、质量控制的标尺。在API分析方法的开发中,需要参考有关化合物或相似化合物分析方法,其次进行杂质的分析工作,并结合工艺本身,以成熟的方法为基础,对分析方法进行逐步优化。
3、原料药及制剂中晶型稳定性研究:考察加速、中间条件,长期条件下的稳定性
在药物临床前研究中,化合物晶型受其他因素(如温度、光照、湿度、压力等)影响会发生转晶现象,导致药物性质发生变化。这意味着从原料药到成品制剂的加工过程中,每道工艺都可能使药物晶型发生改变。因此,研究药物晶型稳定性对于保证药物安全性、有效性十分重要,可以为优势药物晶型的选择、药物制剂处方、制备工艺、药品贮存提供科学依据。
4、原辅料相容性:考察不同条件下原料和辅料相互容纳的能力
原辅料相容性研究在药物研发中至关重要。它确保药物在生产、储存和使用过程中保持稳定,避免化学性质改变、分解或变性等问题。通过合理规划相容性试验,可以减少开发过程中的问题和成本,提高药物的稳定性和安全性。
晶型定性的方法学验证
晶型定性的方法学验证是确保研究结果可靠的重要环节,主要包括专属性、检测限、定量限、重复性和耐用性等方面。专属性验证旨在证明所采用的方法能够准确区分不同晶型,可通过分析含有多种晶型的混合样品,观察各晶型特征峰是否能够清晰分辨且互不干扰来进行验证。
检测限和定量限的确定需通过逐步稀释样品或降低仪器灵敏度,找到能够可靠检测和准确测定晶型的最低浓度。重复性验证是在相同实验条件下,由同一分析人员对同一样品进行多次测定,考察结果的一致性;耐用性验证则是通过改变实验条件(如仪器参数、环境温度等),评估方法对微小变化的耐受程度。只有经过全面且严格的方法学验证,晶型定性研究的结果才能为药物研发和质量控制提供坚实的数据支持。