在药物研发中,原料药存在多晶型现象十分普遍。无论是结晶工艺开发过程中发现了杂质晶型、稳定性考察中监测到晶型转化,还是制剂工艺过程中产生了非预期晶型,一旦确认存在混晶现象,就需要补充定量研究并设定可接受标准。

2025年版《中国药典》四部9015药品晶型研究及晶型质量控制指导原则
《中国药典》2025年版四部9015指导原则也明确要求,申报者需提供充分数据证明对晶型有足够了解和控制。这正是监管审评的关注重点:杂质晶型是否存在风险,仅靠定性判断远远不够。如果早期没有建立定量方法、无法提供充分验证数据,申报阶段大概率就会因缺少定量依据,被药监局要求将杂质晶型检查纳入注册标准。把这类“低含量但高风险”的杂质晶型,从看不见的隐患变成看得见的数据,正是方法开发的核心意义所在。
#1 为什么建议早期引入晶型定量监控策略?
常规研究多依赖于定性的PXRD分析,但要准确评价杂质晶型对药品质量的风险,定性方法的灵敏度往往不足。仅凭“经验推测”,很难满足《中国药典》对RSD、回收率等的验证要求,在审评阶段会带来极大的不确定性与发补风险。
建立晶型药物的质量标准,涵盖晶型种类、纯度、比例及控制标准,既是响应药典指导原则的合规之举,也能从源头主动防控生物利用度波动。早期建立方法所积累的连贯数据,还能为工艺优化提供实时反馈,在面对审评质询时拿出充分的数据链条。
简而言之,不要等到发补通知来了才开始建方法,在药物开发中早期就应该引入并持续完善晶型定量监控策略,通过技术指导原则推荐的PXRD定量分析方法,完成开发与验证,精准控制杂质晶型含量,有效规避发补风险,确保药品顺利获批与上市。
#2 为什么杂质晶型定量是“硬骨头”?
PXRD(粉末X射线衍射)是晶型分析的“金标准”,但它本身是一种体相技术,并不是简单地配个浓度就能直接计算含量的。使用这个技术进行杂质晶型定量真正的难点在于:
样品制备与取向效应:不同晶型颗粒的形态、粒径差异,极易导致制样时产生择优取向。同一个样品倒三次样,特征峰强度可能差别很大,结果不重现;
特征峰的选择与干扰:药用晶型与杂质晶型的衍射峰往往存在重叠。如何找到专属性强、不受其他辅料或晶型干扰的特征峰,是方法成立的前提;
低含量检测的灵敏度与准确度:法规关注的杂质晶型阈值往往很低(如1%或更低),在接近定量限的浓度下,如何保证回收率和RSD达标,对仪器和操作都是巨大考验。

青云瑞晶实验室PXRD设备
#3 发补案例——某原料药中杂质晶型ⅡPXRD定量分析方法开发
在仿制药申报中,制剂中原料药晶型定量数据缺失是一个常见的发补问题,其根本原因在于:生产药品时忽略了定量方法的建立,递交上市资料时该部分研究缺失。
我们服务过的一个真实案例正是如此。
这款原料药存在多晶型现象,药用晶型Ⅰ与杂质晶型Ⅱ共存时存在明确混晶风险,会直接影响药品的生物利用度。客户在申报阶段收到了CDE发补通知:要求将杂质晶型Ⅱ定量检查订入注册标准,并建立定量分析方法、提供验证报告。
针对这个难题,我们严格按照定量方法学开发推进:首先针对药品进行了制样与扫描参数的优化,随后配制0%~100%的梯度样品,绘制出线性优良的校正曲线(R² = 0.9996)。通过这种方式建立了基于PXRD特征峰的杂质晶型定量分析方法,并完成了全面方法学验证。该方法有效测定了低至1%的杂质晶型Ⅱ,最终成功帮助该客户完成了补充注册申报工作。
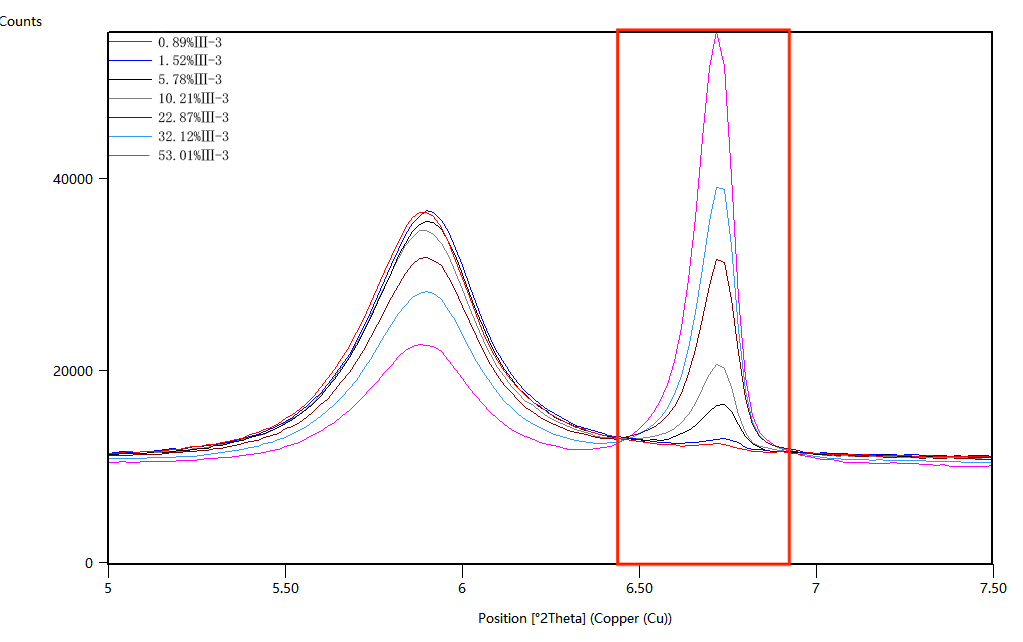
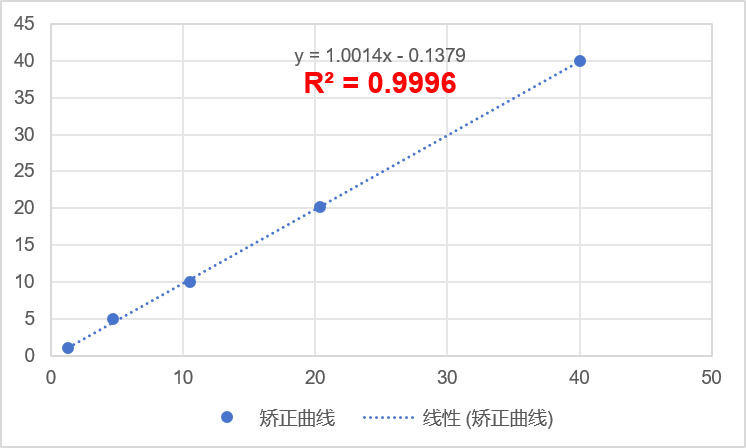
不同比例晶型Ⅱ的PXRD谱图 晶型Ⅱ定量分析的矫正曲线
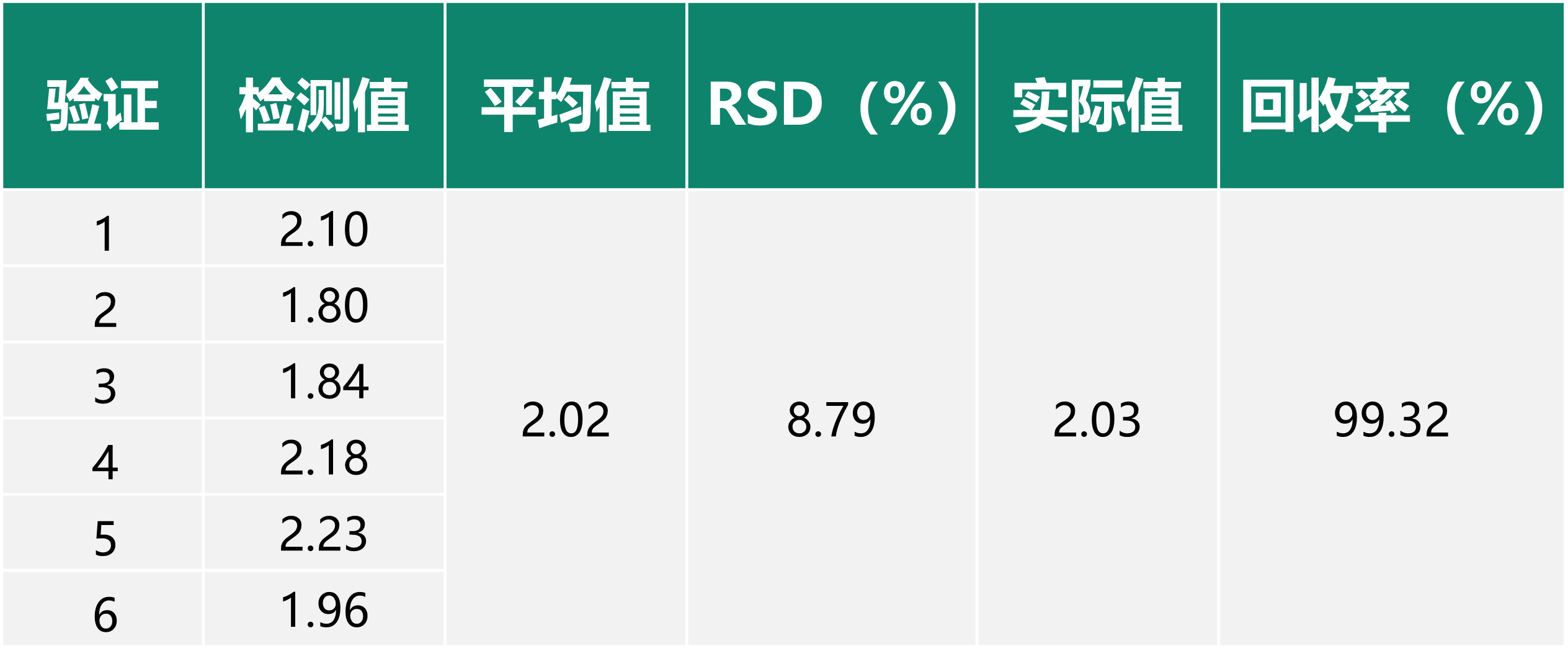
方法学验证数据
#4 青云瑞晶药物固态性质分析服务
在药物开发中遇到晶型定性或定量难题时,早期引入并持续完善晶型监控策略,是从源头规避生物利用度波动、免于发补风险的关键。青云瑞晶深耕药物固态研究领域,具备丰富的CDE发补案例应对经验,可为药企提供从方法开发、验证到申报支持的一站式药物晶型定性与定量服务。
药物固态性质分析服务:
原料药理化性质检测
晶型定性分析
晶型定量分析
如果您在药物研发中正面临复杂的混晶风险,或需要对特定杂质晶型建立精准的质控方法,欢迎联系我们获取更多完整的项目案例详情与定制化技术解决方案。




















