前言
9p21染色体区域的大片段缺失在多种癌症中十分常见。当该区域的抑癌基因CDKN2A丢失时,相邻的MTAP和FOCAD基因通常也共同缺失。其中,FOCAD缺失约占所有MTAP缺失肿瘤的三分之一,在非小细胞肺癌、胰腺癌等难治性癌症中尤为突出。
FOCAD 的主要作用是稳定细胞内的mRNA质控系统,帮助清除异常RNA、维持正常蛋白翻译。而FOCAD缺失型肿瘤细胞会高度依赖HBS1L/PELO 核糖体救援通路维持存活,形成独特的合成致死依赖关系。然而,HBS1L与另一个重要蛋白GSPT1高度同源,传统药物难以区分两者,此前一直没有高选择性靶向HBS1L的小分子药物。
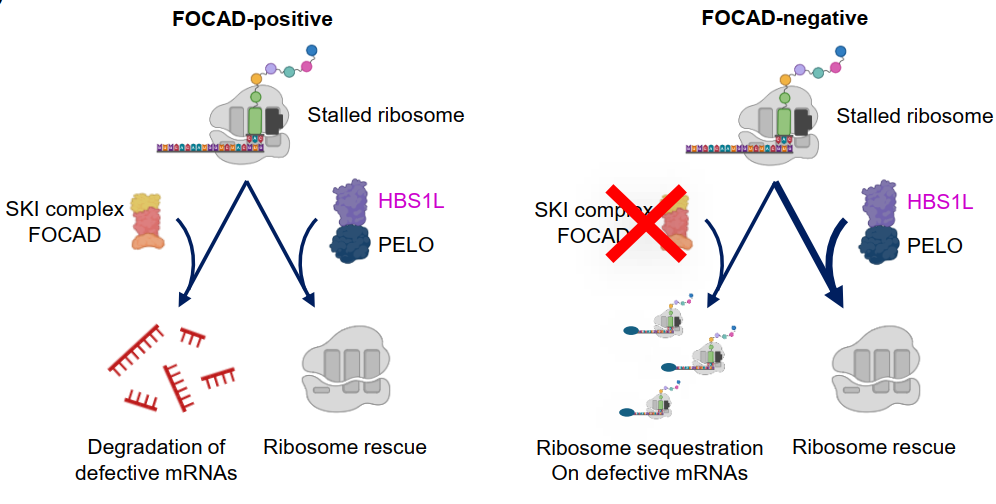
FOCAD失活与HBS1L/PELO复合物之间合成致死相互作用的治疗假说模型
Tango Therapeutics是一家临床阶段精准肿瘤学公司,核心策略是利用“合成致死”原理开发针对特定基因突变癌症的靶向药物。TNG961 是其针对 FOCAD 缺失肿瘤研发的口服选择性 HBS1L 分子胶降解剂,目前已完成 IND 支持性研究,安全性良好,具备进入临床开发的条件。
近日,Tango公司的Hilary E. Nicholson等研究人员报道了TNG961 的发现、优化与临床前研究,核心成果包括:
机制创新:首次验证FOCAD 缺失与HBS1L 的合成致死关系,为9p21 共缺失肿瘤提供新靶点;
药物创新:开发首个高选择性HBS1L 降解剂,强效降解HBS1L 且不影响GSPT1 等同源蛋白;
药效突破:口服TNG961 可消退FOCAD 缺失肿瘤,对PRMT5 抑制剂耐药肿瘤依然有效,具备临床互补价值。
相关研究以“TNG961 is a selective oral HBS1L molecular glue degrader for the treatment of FOCAD-deleted cancers”为题,4月19日在线发表于《Cancer Discovery》。值得一提的是,TNG961的IND研究已经做完,临床前景明确,这让本研究更有现实意义,为难治癌症治疗打开了新方向。

研究内容
药物筛选并优化得到TNG961
研究团队通过建立"细胞HiBiT降解+TR-FRET三元复合物"双轨并行的筛选策略,获得了初始苗头化合物TNG-6266。随后,利用冷冻电镜结构指导理性药物优化,最终得到了候选分子TNG961。
该分子可以在强效诱导 HBS1L 降解的同时,完全不影响结构高度同源的 GSPT1,实现了理想的靶点选择性。
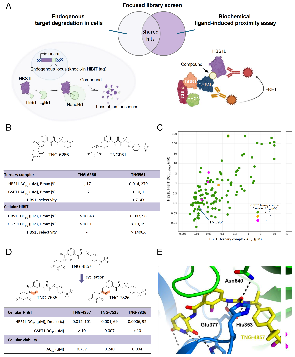
图2. 筛选策略与分子胶的发现
TNG961作用机制:CRBN依赖的选择性蛋白降解
冷冻电镜结构(2.9 Å)揭示,TNG961 作为分子胶,能够稳定E3泛素连接酶CRBN与HBS1L之间的结合,促使HBS1L泛素化并被蛋白酶体降解。整个过程依赖 CRBN 与 NEDD8 通路。
全蛋白质组证实,TNG961仅直接降解 HBS1L,不影响其他常见底物,显示出高度选择性,安全性良好。
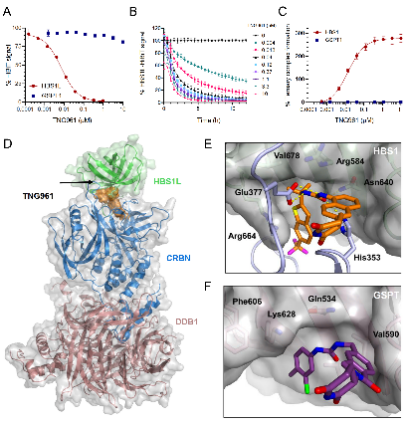
图3. TNG961 介导三元复合物形成与降解机制
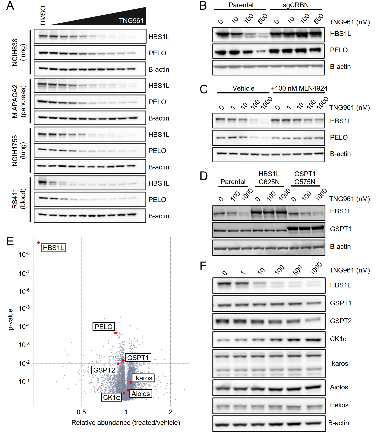
图4. TNG961 可强效、选择性地通过 CRBN 通路降解 HBS1L
FOCAD 依赖性功能验证:精准杀伤缺失型肿瘤细胞
在多组等基因细胞对中,团队发现TNG961对FOCAD阴性细胞具有强抑制活性,对 FOCAD 阳性细胞影响极小,选择性抑制倍数超过100倍。大规模细胞谱筛选确认,FOCAD缺失是最主要的敏感标志物,与肿瘤组织类型无关。
机制研究表明,TNG961选择性诱导FOCAD阴性细胞翻译停滞、内质网应激与未折叠蛋白反应,最终导致了细胞死亡。
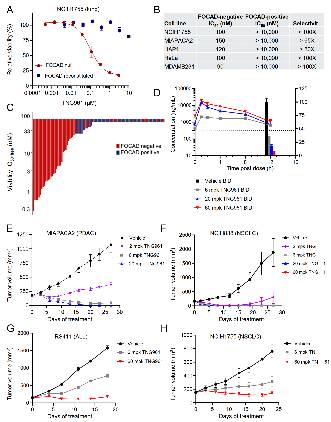
图5. TNG961 在体外选择性抑制FOCAD阴性细胞的存活,并在体内抑制FOCAD阴性肿瘤的生长。
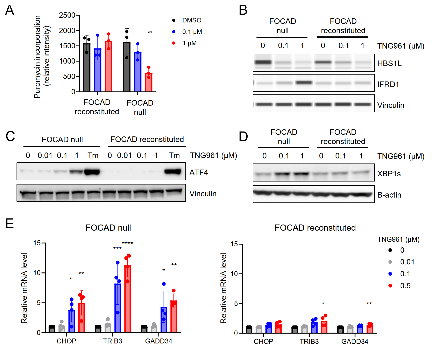 图6. TNG961 可选择性地在FOCAD缺失细胞中引发翻译停滞,并激活内质网应激与未折叠蛋白反应。
图6. TNG961 可选择性地在FOCAD缺失细胞中引发翻译停滞,并激活内质网应激与未折叠蛋白反应。
临床转化潜力:口服有效且可克服 PRMT5 抑制剂耐药
口服TNG961在胰腺癌、肺癌、血癌等多种FOCAD缺失模型中均可诱导肿瘤消退,且对PRMT5抑制剂耐药的模型同样有效;FOCAD蛋白C端截短≥15个氨基酸即可赋予其对TNG691的敏感性,这有望扩大潜在患者人群,支持以 FOCAD 缺失/截短作为伴随诊断生物标志物,开展精准临床开发。
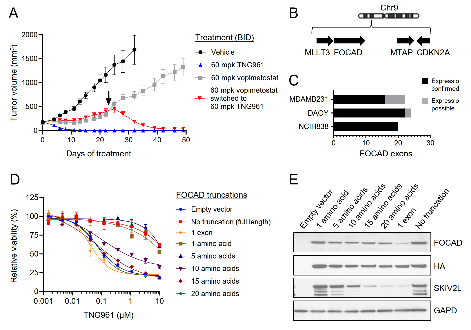
图7. TNG961在PRMT5抑制剂耐药模型中仍具体内抗肿瘤活性,并可抑制携带FOCAD蛋白C端截短的细胞生长。
总结
TNG961作为首个高选择性HBS1L分子胶降解剂,成功解决了HBS1L与GSPT1的同源性难题,并在多种临床前模型中实现了肿瘤消退。尤为重要的是,该药对PRMT5抑制剂耐药的肿瘤依然有效,且FOCAD C端小片段截短即可赋予敏感性,显著扩大了可适用的潜在患者人群。




















