前言
RAS是肿瘤中最常见的致癌驱动基因之一,其突变会导致细胞持续增殖。针对RAS的靶向治疗长期面临挑战。近年来发展出的三复合物抑制剂(TCI)是一种新型分子胶药物,其作用方式是结合处于激活状态的RAS蛋白,并同时招募细胞内的亲环蛋白A(CYPA),三者形成一个人工三元复合物。这个复合物会阻断RAS与下游效应蛋白(如RAF)的结合,从而抑制致癌信号。
Daraxonrasib 就是一种能同时靶向多种RAS突变体的TCI,在临床试验中已显示出初步疗效。然而,和多数靶向药物一样,耐药问题随之出现,但是此前对这类分子胶药物的耐药机制研究尚不明确,成为制约其临床转化与长期获益的关键瓶颈。
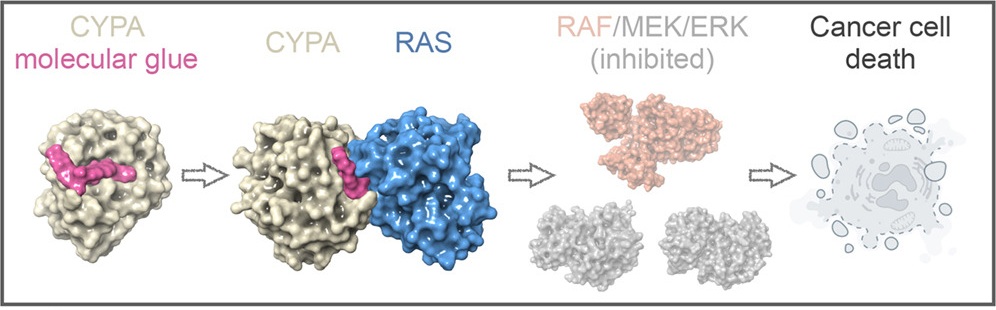
图. Daraxonrasib 的分子胶机制
近日,美国纪念斯隆凯特琳癌症中心(MSK)的Piro Lito等相关研究人员首次系统揭示了RAS靶向分子胶药物——三复合物抑制剂(TCIs)的临床耐药机制,并给出了针对性解决方案。这项研究为破解RAS突变癌症的长期治疗难题提供了关键科学蓝图。
相关研究以“Disrupted molecular glue complex drives RAS inhibitor resistance”为题,5月5日在线发表于《Cell》上。

研究内容
患者及临床前模型中的耐药改变
研究团队对40例接受daraxonrasib治疗的RAS突变癌症患者进行了配对样本测序,在45%的患者治疗后样本中发现获得性改变,包括KRAS Y64C/D点突变、BRAF激酶失活突变以及KRAS基因扩增等。
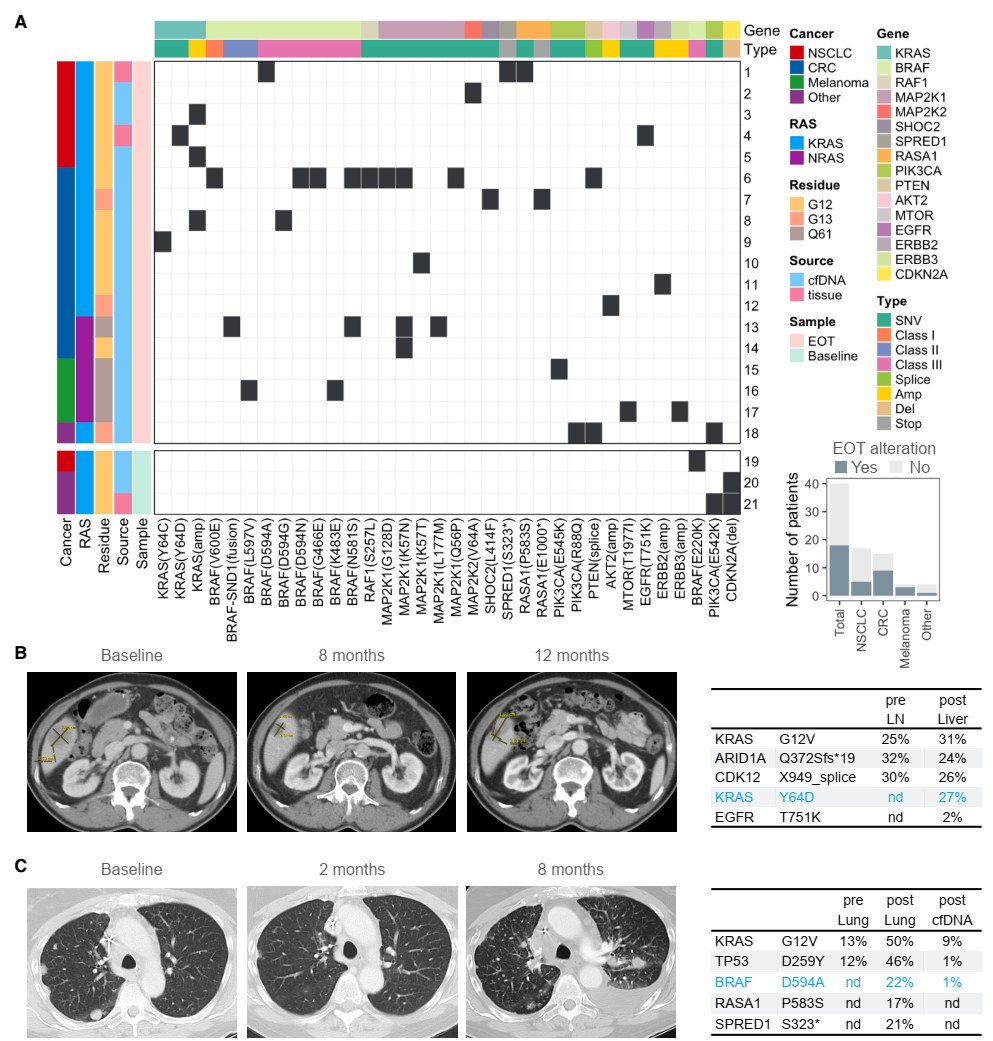
图1. RAS(ON)抑制剂Daraxorasib治疗患者的耐药性改变
与此同时,高通量CRISPR碱基编辑筛选和长期药物筛选在临床前模型中独立鉴定出一致的耐药位点,主要位于KRAS Switch II区域(Y64、Y71)及CYPA药物结合界面,两者结果相互印证。
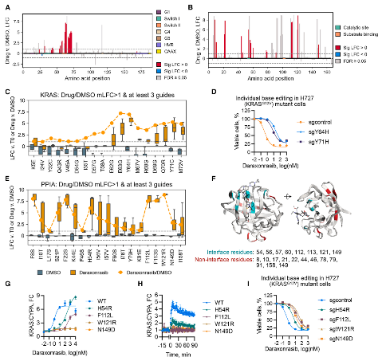
图2. 碱基编辑筛选鉴定破坏KRAS‑CYPA三元复合物的变异
三类关键耐药机制
1. KRAS Y64突变:直接破坏药物结合
机制研究显示,KRAS Y64 突变通过破坏药物与RAS之间关键的π-π 堆叠作用,直接削弱三重复合物形成,使药物无法有效阻断 RAS-RAF 结合并抑制ERK信号。
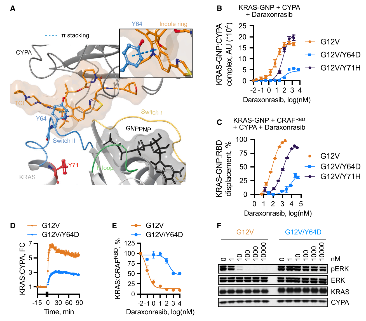
图3. KRAS Y64突变通过正构机制削弱daraxonrasib结合
2. KRAS Y71H突变:增强RAS-RAF亲和力
与Y64不同,Y71H并不直接影响药物结合,但显著增强了KRAS与RAF RBD的亲和力;晶体结构揭示H71与CRAF RBD中的R67形成了新的氢键和π-阳离子相互作用,这种新作用界面使RAF更难被CYPA从RAS上置换,从而导致耐药。
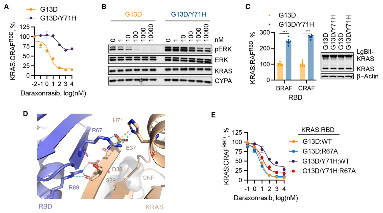
图4. KRAS Y71H通过新作用界面增强对RAF的亲和力
3. 激酶失活/低活性BRAF突变:通过RAF二聚化抵抗
进一步实验证实,激酶失活/低活性BRAF Ⅲ 类突变可驱动耐药,且该作用依赖完整的RAF二聚化与RAS结合能力;这类突变体不易被药物从RAS上置换,并会干扰药物招募CYPA到RAS上。
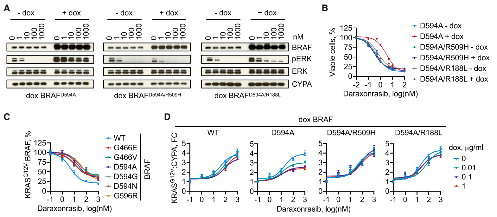
图5. 激酶失活 BRAF 突变削弱 CYPA 招募并导致耐药
利用化学诱导二聚化系统证明,单纯诱导RAF二聚化就足以模拟III类BRAF突变的耐药表型。二聚化使RAF的CRD结构域更牢固地结合KRAS,而破坏CRD与KRAS结合的突变可逆转此耐药。
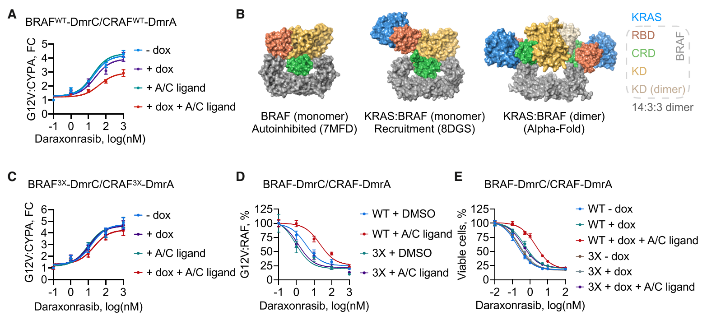
图6. RAF二聚化通过CRD结构域削弱分子胶功能
破解耐药的针对性解决方案
1. 应对Y64突变:一种新型TCI(RMC‑4791)
基于结构指导,团队成功筛选并验证了一种能有效靶向Y64突变型RAS的新型三复合物抑制剂RMC-4791,为这部分患者提供了新的治疗选择。
RMC‑4791以不同模式与RAS结合,对Y64突变的依赖性显著降低。实验表明该化合物能有效抑制KRAS Y64突变体的信号和增殖,效果优于daraxonrasib。
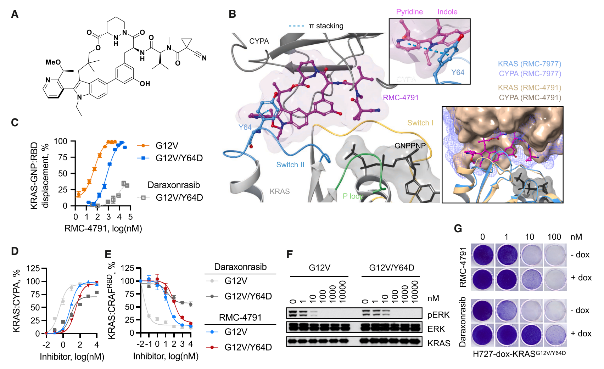
图7. 可将CYPA招募至Y64突变KRAS的抑制剂
2. 应对BRAF突变:联合治疗策略
针对BRAF驱动的耐药,团队发现将daraxonrasib与RAF二聚体抑制剂、MEK抑制剂或ERK抑制剂联用,可显著恢复药物敏感性,在动物模型中有效抑制耐药肿瘤生长。
总结
这项研究系统揭示了RAS分子胶抑制剂daraxonrasib的耐药机制:
· KRAS Y64C/D(直接破坏药物结合)
· BRAF 激酶失活突变(D594A/G/N 等 Ⅲ 类突变)
· KRAS Y71H(增强 RAS-RAF 结合)
· CYPA 突变(临床暂未普遍检出)
这些机制看似分散,实则殊途同归:阻碍药物成功招募CYPA形成三元复合物。
更重要的是,它不仅解释了“为什么失效”,还前瞻性地给出了“如何应对”的解决方案,即通过开发下一代抑制剂或采用合理的联合用药来破解耐药。
晶体结构解析在本研究中发挥了关键作用。它直接确定了Y64与药物的π-π堆积作用,证明Y64突变破坏药物结合;同时解析了Y71H与RAF RBD的新形态相互作用,解释了该突变为何增强RAS-RAF亲和力。此外,结构还指导了RMC-4791的设计,证实其结合模式不同于daraxonrasib,从而能够规避Y64突变。




















