前言
抗生素耐药性问题日益严峻,亟需开发作用于新靶点的抗生素。肽聚糖生物合成通路是抗菌药物的经典靶点,MurJ 作为脂质II翻转酶,通过交替访问机制(Alternating Access Mechanism)将脂质II底物从细胞质翻转到周质,是细菌细胞壁生物合成中一个极具前景但尚未被充分开发的抗菌靶点 。
目前已知仅有的革兰氏阴性菌 MurJ 抑制剂是来自单链 RNA 噬菌体M和PP7的单基因裂解蛋白 (Sgls),分别称为 Sgl™ 和 SglPP7 。解析这些天然噬菌体抑制剂与MurJ的作用机制,不仅有助于理解噬菌体-宿主的进化博弈,更为开发靶向MurJ的新型抗菌药物提供了宝贵的结构线索。
近日,加州理工学院William M. Clemons Jr教授团队解析了 MurJ 结合 Sglᴹ、Sglᴾᴾ⁷的冷冻电镜结构,还发现并表征了第三种靶向 MurJ 的噬菌体裂解蛋白。研究揭示了它们殊途同归的抑制机制,明确了MurJ上一个可用于药物设计的共同结合位点,为对抗耐药菌的新型抗生素研发提供了关键分子基础。
相关研究以“Convergent MurJ flippase inhibition by phage lysis proteins”为题,于2月25日在线发表于《Nature》上。

研究内容
1. Sglᴹ-MurJ 复合物结构
Sglᴹ-MurJ 复合物冷冻电镜显示Sglᴹ通过的跨膜螺旋紧密结合在TM2/TM7界面附近的凹槽,将MurJ锁定在周质开放(向外)构象。通过突变实验验证了结合界面上的关键氨基酸对裂解功能至关重要。
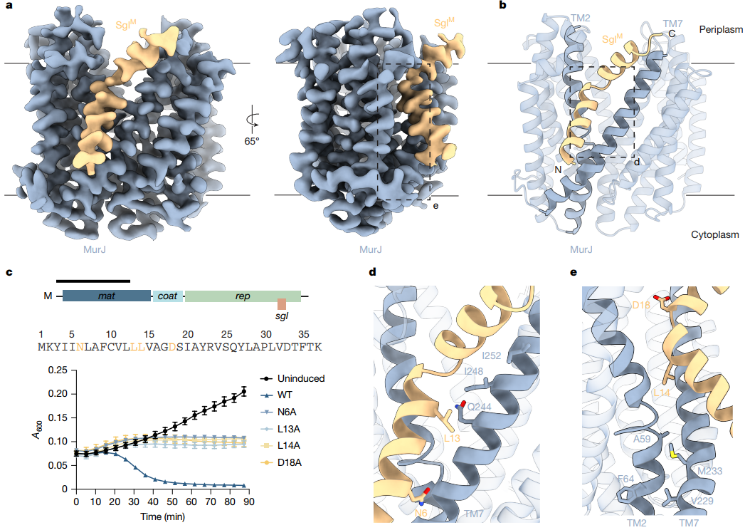
图1. Sglᴹ-EcMurJ复合体的结构(分辨率3.6 Å)
值得一提的是,为了克服 MurJ 缺乏跨膜外结构域且体积较小(55 kDa)导致的电镜解析困难,研究人员在其 N 端融合了 BRIL 蛋白,并添加了抗BRIL的Fab抗体及抗Fab纳米抗体以辅助颗粒对齐,最终成功用冷冻电镜得到了MurJ和与三种不同的 Sgl 结合的复合物结构。
此外,研究还验证了 EcMurJBRIL能完全互补 MurJ 敲除菌株的生长,且过表达后可拯救 Sgl 介导的细菌裂解,说明该融合蛋白保留了 MurJ 的天然生物学功能,保证了复合物结构的生理真实性。
2. Sglᴾᴾ⁷-MurJ 复合物结构
Sglᴾᴾ⁷与MurJ 复合物结构显示,MurJ 同样处于周质开放构象,Sglᴾᴾ⁷的跨膜螺旋结合在 MurJ TM2/TM7 区域,且其 C 端以有序延伸构象深入MurJ中央空腔,形成有序的延伸构象。关键残基突变验证显示,Sglᴾᴾ⁷的 Tyr36(结合 TM2/TM7)和 C 端残基(Pro49、Ile50、Trp53)对裂解活性至关重要,MurJ 的 Q244P 耐药突变同时抵抗 Sglᴹ和 Sglᴾᴾ⁷,证实二者结合 MurJ 的同一界面。
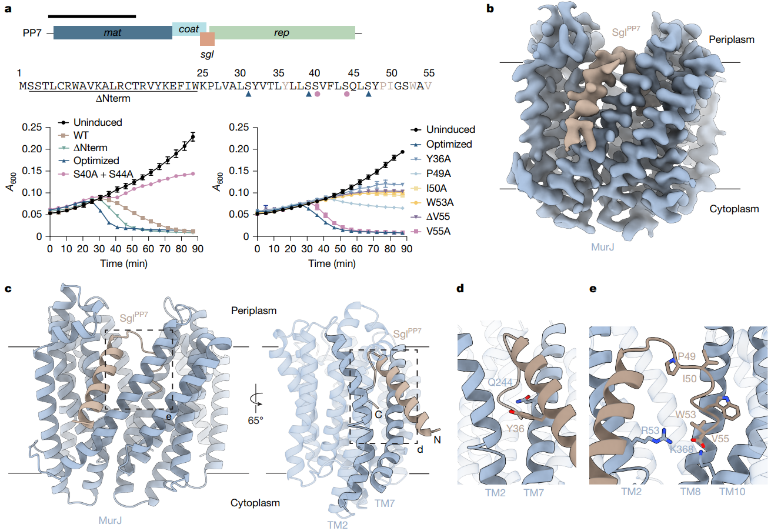
图2. Sglᴾᴾ⁷-EcMurJ 复合物的结构(分辨率3.7 Å)
3. 发现第三种趋同进化的 Sglᴄᴊ³
研究从环境宏转录组数据预测的长江3号噬菌体中,鉴定出第三种趋同进化的 Sglᴄᴊ³,证实其靶点为 MurJ;解析冷冻电镜复合物结构发现 MurJ 呈周质开放构象,Sglᴄᴊ³ 结合于 MurJ 的 TM2/TM7 区域,结合模式与 Sglᴾᴾ⁷相近,其跨膜区和 C 端螺旋的特定残基为结合关键,MurJ 的 Leu50Trp 突变会通过空间位阻抑制二者结合。
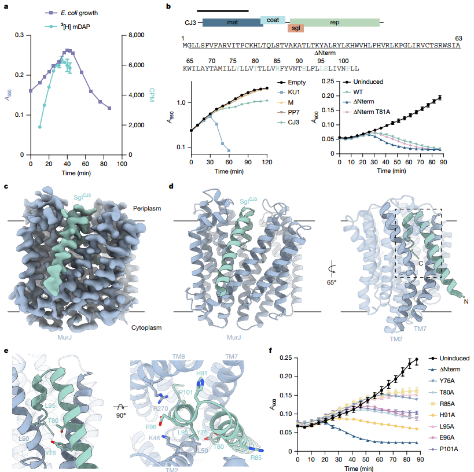
图3. SglC³ 的发现及 SglC³-EcMurJ 复合物的结构(3.6 Å 分辨率)
4. 三种 Sgl 的趋同抑制机制与药物靶点挖掘
将三种Sgl-MurJ复合物结构进行叠加比较发现,尽管Sgl的C末端结构各异,但它们的跨膜螺旋都结合在同一个位点,并且都利用负电荷残基与MurJ腔内的保守正电荷残基相互作用。这个由TM2、7、8构成的腔体,含有多个高度保守的极性残基,构成了一个非常有潜力的“可成药口袋”。
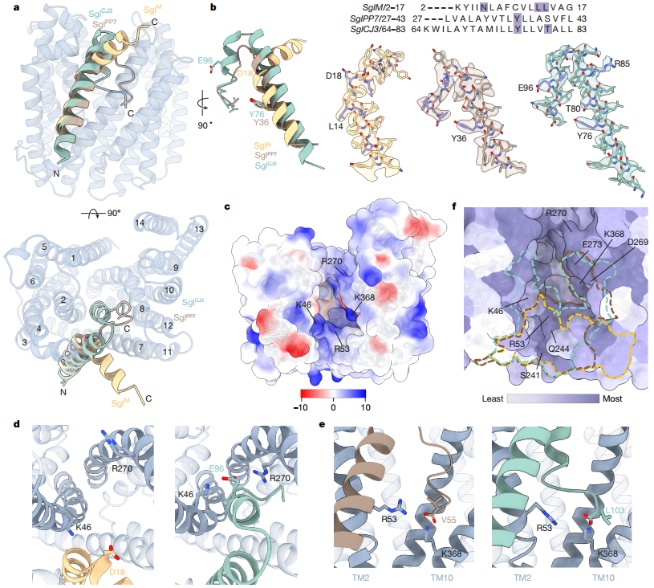
图4. Sgl 结合的 MurJ 结构比较
总结
本研究通过冷冻电镜技术成功解析了三种起源不同、序列各异的噬菌体裂解蛋白(Sglᴹ、Sglⁿᵖ⁷、Sglᶜᴶ³)与细菌靶点 MurJ 的复合物高分辨率结构,首次发现这些蛋白通过趋同进化,均结合在 MurJ 的 TM2-TM7 保守界面,并将 MurJ 稳定锁定在周质开放构象,直接阻断其构象转换和脂质 II 转运功能。
结构分析进一步表明,Sglⁿᵖ⁷和 Sglᶜᴶ³ 的 C 末端深入 MurJ 中央空腔,与腔内保守的带正电荷残基形成关键静电相互作用,而这些残基本身对 MurJ 的翻转酶活性至关重要。该研究不仅阐明了噬菌体 Sgl 蛋白抑制 MurJ 的分子机制,填补了目前革兰氏阴性菌 MurJ 与抑制剂相互作用的结构空白,还进一步证实 MurJ 是极具潜力的广谱抗菌靶点。
研究解析的 Sgl-MurJ 复合物结构为基于结构的 MurJ 靶向小分子抑制剂设计提供了精准模板,而噬菌体 Sgl 的趋同进化特征也为挖掘新型抗菌肽、开发新型抗菌疗法奠定了重要基础,对解决当前全球面临的抗菌药物耐药性问题具有重要的理论研究和临床应用价值。



















