前言
CRISPR-Cas9是当前应用最广泛的基因编辑工具,但其脱靶效应仍是制约其治疗应用的主要瓶颈。虽然已有多种高保真Cas9变体被开发出来,但这些设计大多基于线性DNA底物,忽略了细胞内DNA天然的拓扑结构。
负超螺旋是DNA在转录、复制等过程中常见的物理状态,已有研究表明它能显著增强Cas9的脱靶活性,但其分子机制一直缺乏结构层面的解析。因此,阐明负超螺旋如何调控Cas9对靶标和脱靶位点的识别,对于深入理解Cas9在细胞内的行为、以及设计更安全的基因编辑工具具有重要意义。
近日,Imperial College London 的 David S. Rueda 团队等研究人员通过解析负超螺旋DNA上Cas9的冷冻电镜结构,揭示了负超螺旋通过诱导HNH结构域向催化构象摆动并降低R-loop形成能垒,从而增强脱靶活性的分子机制。这一发现为设计下一代高保真基因编辑工具提供了关键结构基础。
相关研究以“Structural basis of supercoiling-induced CRISPR–Cas9 off-target activity”为题,于3月25日在线发表于《Nature》。

研究内容
创新方法:负超螺旋DNA小环的构建
为了阐明(−)SC在Cas9靶标识别、变构激活和切割中的作用,研究团队突破常规,创新性地构建了携带负超螺旋的DNA微环(minicircle)底物。
切割实验显示,负超螺旋不仅显著加速Cas9对靶向位点的切割,更让原本在线性底物上无法切割的脱靶位点也被高效剪切。AFM进一步揭示,负超螺旋使DNA微环从开放结构转变为更为紧缩且伴有局部缺陷的构象,而Cas9结合后可使DNA恢复为开放环状结构,表明Cas9利用了底物中储存的拓扑能量来辅助局部解链和R-loop组装
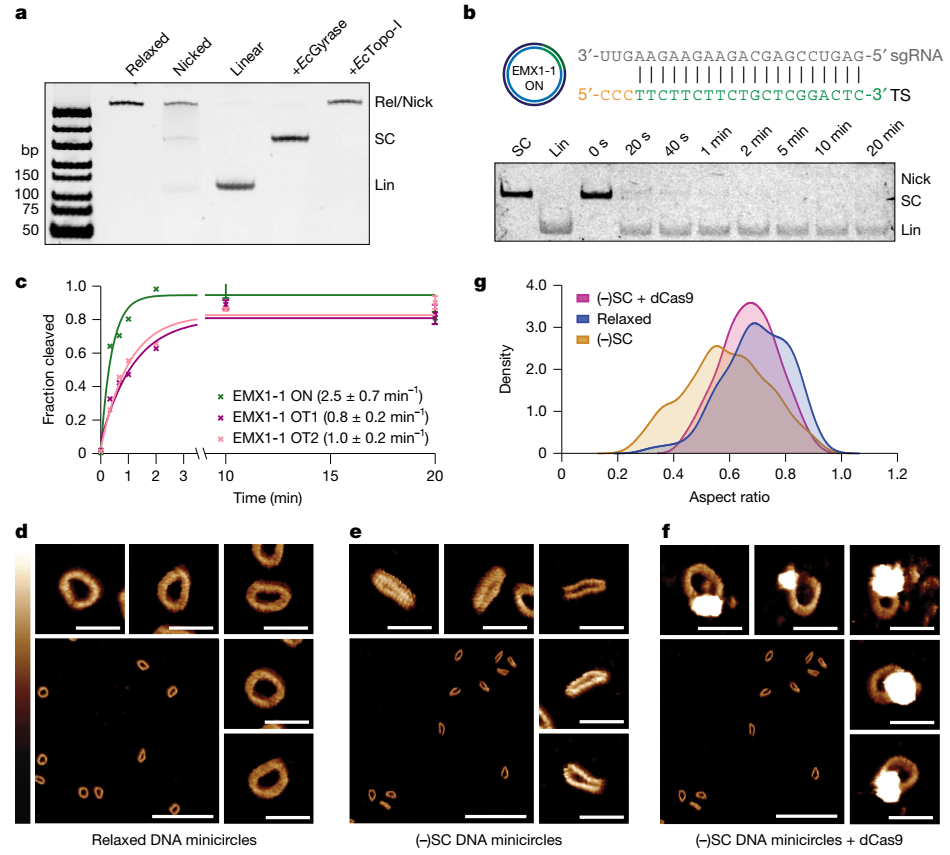
图1. 负超螺旋DNA微环的合成与表征
冷冻电镜结构揭示分子机制
冷冻电镜解析发现,Cas9 结合负超螺旋靶标 DNA 时,HNH 结构域向靶链切割位点摆动 15 Å,处于更接近催化的活性构象,同时 R-loop 的 PAM 远端区域结构柔性增加,非靶链的完整结合路径也首次被清晰解析。
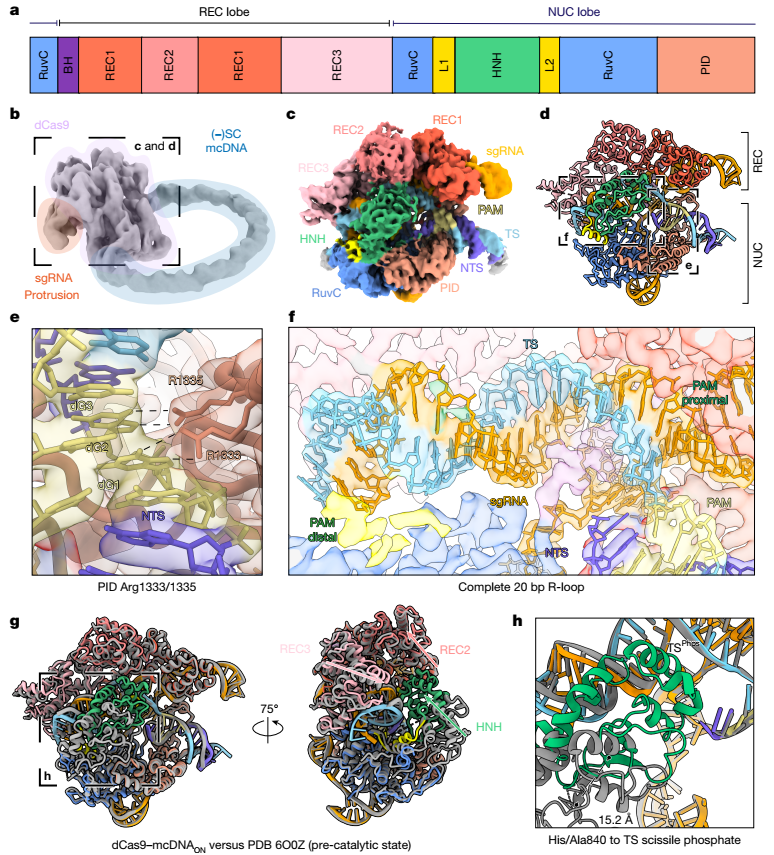
图2. 靶向负超螺旋DNA上dCas9的冷冻电镜结构
接着,研究团队解析了dCas9与含有多个错配的脱靶小环OT1(含有包括种子区在内的5个错配)的复合物结构(分辨率2.6 Å)。结构揭示,Cas9能够通过多样的策略适应整个原间隔序列中的错配。
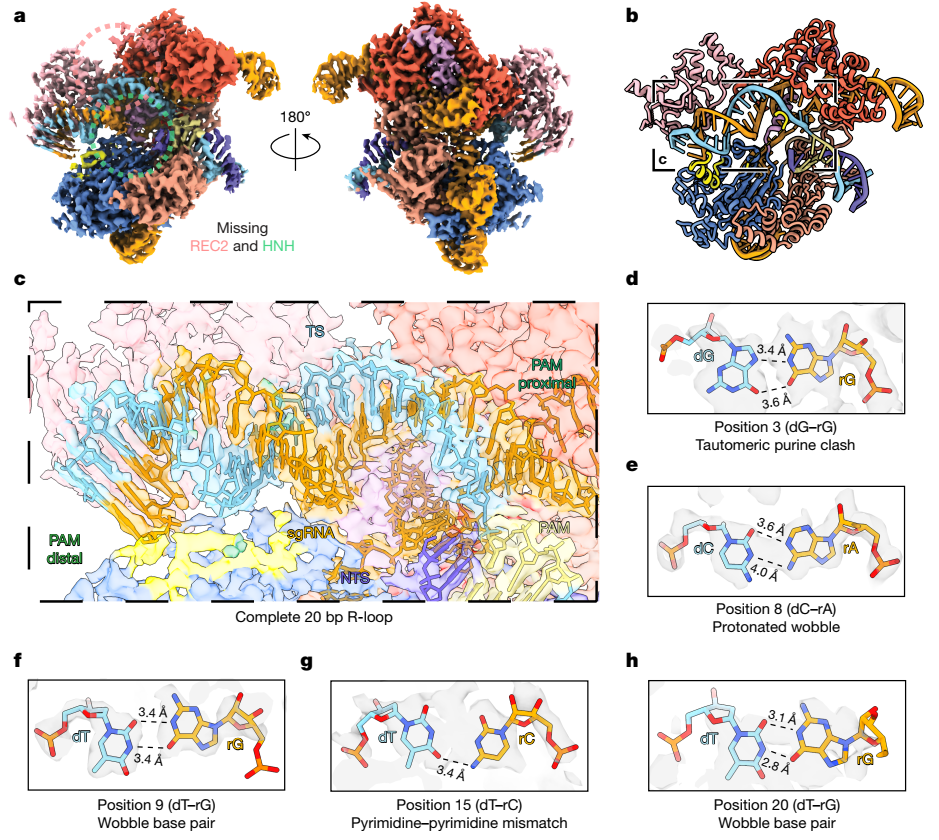
图3. 脱靶OT1负超螺旋DNA上dCas9的冷冻电镜结构
对于主要含有PAM远端错配的脱靶小环OT2,结构(分辨率3.9 Å)显示了一个惊人的发现:PAM 远端的 R 环区域因结构柔性过高无法解析,仅能清晰分辨出 PAM 近端的 11 个碱基对。这提示,在负超螺旋底物上,完整的R-loop形成可能并非切割所必需。结合截短gRNA切割实验进一步证实,仅需14 bp的R-loop即可激活切割”。
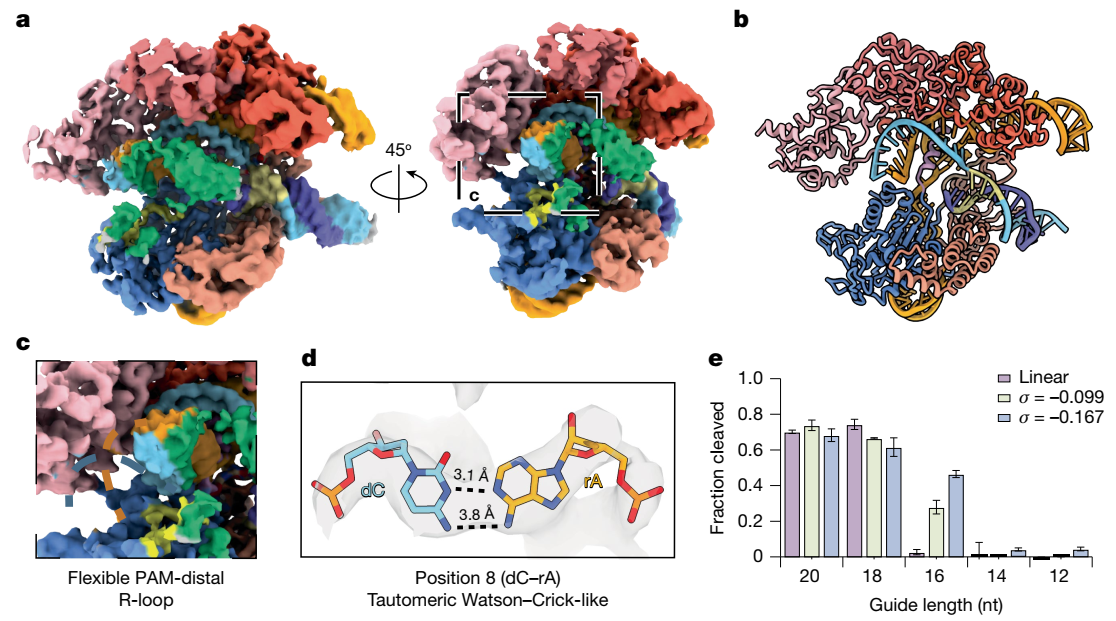
图4. dCas9 与 OT2 型负超螺旋 DNA 微环复合物的冷冻电镜图及分子模型
单分子FRET揭示的HNH动态
研究团队结合了光镊与荧光共振能量转移技术,结果显示负超螺旋通过调控 HNH 结构域的柔性与定位,变构激活 Cas9 的脱靶切割,且降低了 DNA 解旋和 R-loop 形成的能垒。
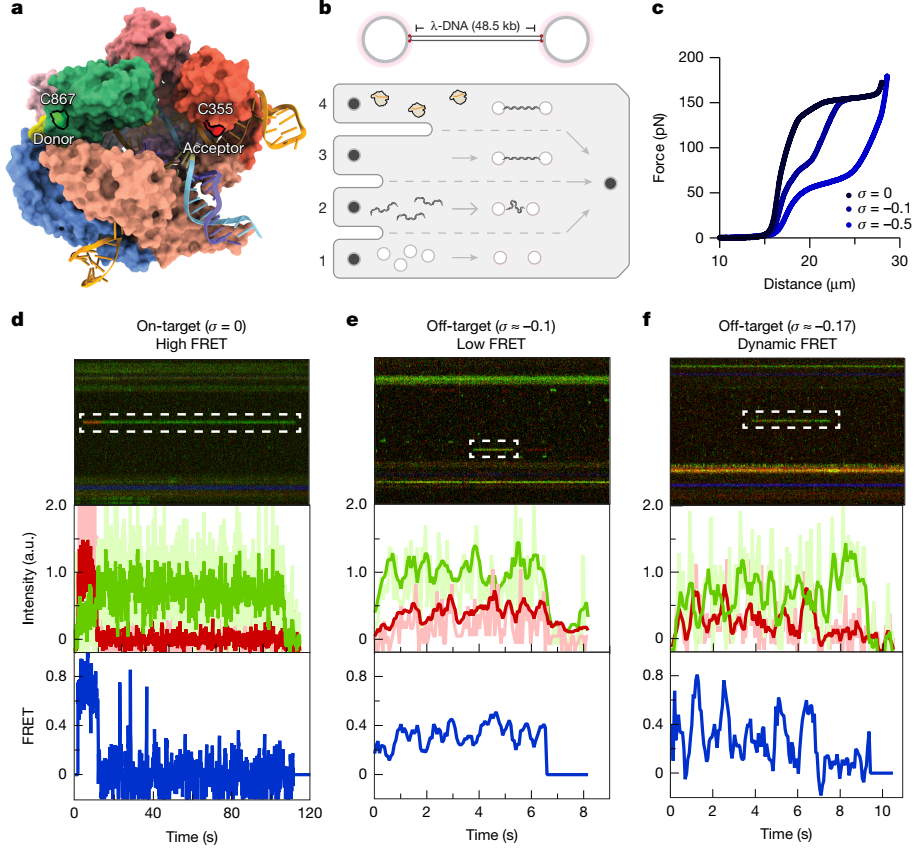
图5. 单分子光镊-FRET揭示HNH结构域构象动态
高保真突变体测试
现有高保真变体(如SuperFi、Sniper2L)均基于线性DNA底物开发,未充分考虑细胞内DNA超螺旋的拓扑特征。实验表明,在负超螺旋底物上,这些变体仍可切割脱靶位点,提示其特异性在拓扑约束条件下可能受限。
总结
这项研究首次系统揭示了负超螺旋诱导 CRISPR-Cas9 脱靶的分子机制:负超螺旋改变 DNA 结构并降低其解旋能垒,使 Cas9 的 HNH 结构域呈高催化活性构象,同时增强 R-loop 柔性,让 Cas9 通过新型非经典碱基配对容纳各类错配,且PAM远端仅需 14 bp 的 R-loop 即可激活切割,大幅降低了序列识别的严格性。
该研究填补了 DNA 拓扑结构调控 Cas9 活性的分子机制空白,从应用层面看,研究结果为下一代高保真CRISPR效应器的设计提供了结构基础——提示未来在优化Cas9特异性时,需将其在细胞内真实拓扑环境中的行为纳入考量,而非仅依赖线性底物的筛选策略。此外,研究中建立的负超螺旋DNA微环平台也为其他DNA结合蛋白的拓扑依赖性研究提供了可借鉴的技术范式。




















