前言
遗传性酪氨酸血症I型(HT1)由延胡索酰乙酰乙酸水解酶(FAH)功能丧失引起,FAH是酪氨酸分解代谢途径中的第五个酶,其功能缺失会导致有毒代谢物在体内堆积,所以HT1患者会有严重的肝肾损伤问题,甚至会患肝癌。目前临床上使用的药物尼替西农( Nitisinone)虽然可以通过抑制上游酶来阻止有毒代谢物的生成,但无法恢复FAH的功能,因此会带来酪氨酸蓄积、代谢负担等问题。
因此,亟需开发新的治疗策略。小分子药理学伴侣是一类特殊的小分子药物,它们不直接抑制或激活酶的活性,而是通过帮助易错误折叠的蛋白质维持其正确的三维结构,从而恢复或改善蛋白功能。由于FAH中有害突变的主要机制是蛋白质稳态受损,因此可以使用药理学伴侣来提高其酶活性。
近日,西班牙ATLAS分子制药公司Oscar Millet等研究人员基于人源FAH蛋白晶体结构,合理设计、筛选并优化得到小分子药理学伴侣,其可以结合并稳定突变型FAH蛋白(G337S),为遗传性酪氨酸血症I型提供了全新治疗策略与候选药物,弥补了尼替西农的治疗短板,具备罕见病精准治疗的重大转化价值。
针对酪氨酸血症I型(Tyrosinemia type I)的药理学伴侣研发是ATLAS公司的管线项目,代号ATL-002,目前该项目正处于先导化合物验证阶段,具备明确的产业化布局前景。
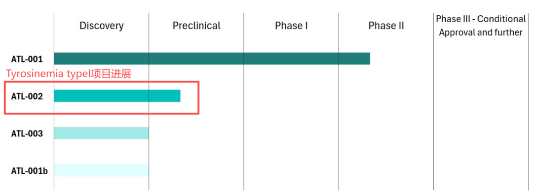
图片来源:ATLAS官网
最新研究成果以“Rational Design of Small-Molecule Stabilizers of Human Fumarylacetoacetate Hydrolase for the Treatment of Tyrosinemia Type I”为题,5月13日在线发表于《Journal of Medicinal Chemistry》上。

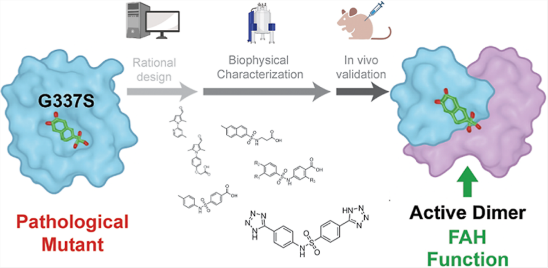
研究内容
人源FAH晶体结构解析与初始片段的发现
研究团队首先解析了人源FAH与产物乙酰乙酸的高分辨率晶体结构(1.9 Å),发现FAH以同源二聚体形式存在,活性中心结合一个钙离子,该结构为后续药物设计提供了精确模板。
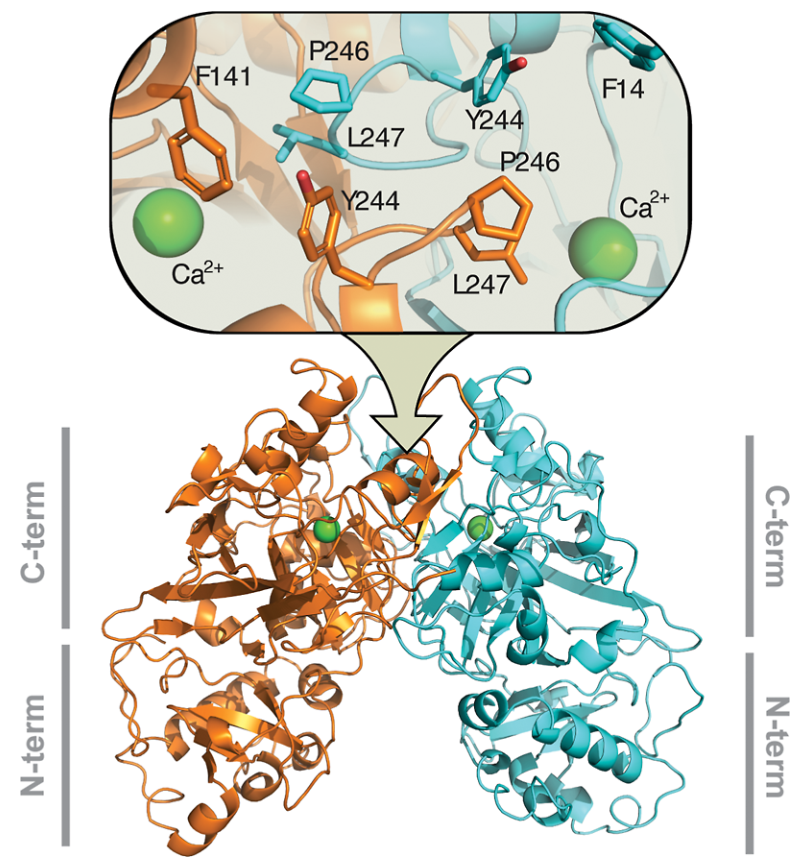
图2. 人源FAH蛋白的晶体结构(PDB: 9T9X,分辨率1.9 Å)
依托此结构,团队对化合物库开展虚拟对接,经NMR、ITC验证得到初始片段S0,其通过π-π堆积结合于口袋入口的Phe141和Tyr244;随后保留该芳香堆积特征并引入可配位钙离子的羧酸基团进行定向生长,将亲和力提升约400倍,得到先导化合物S1.1(Kd = 1.3 μM)。
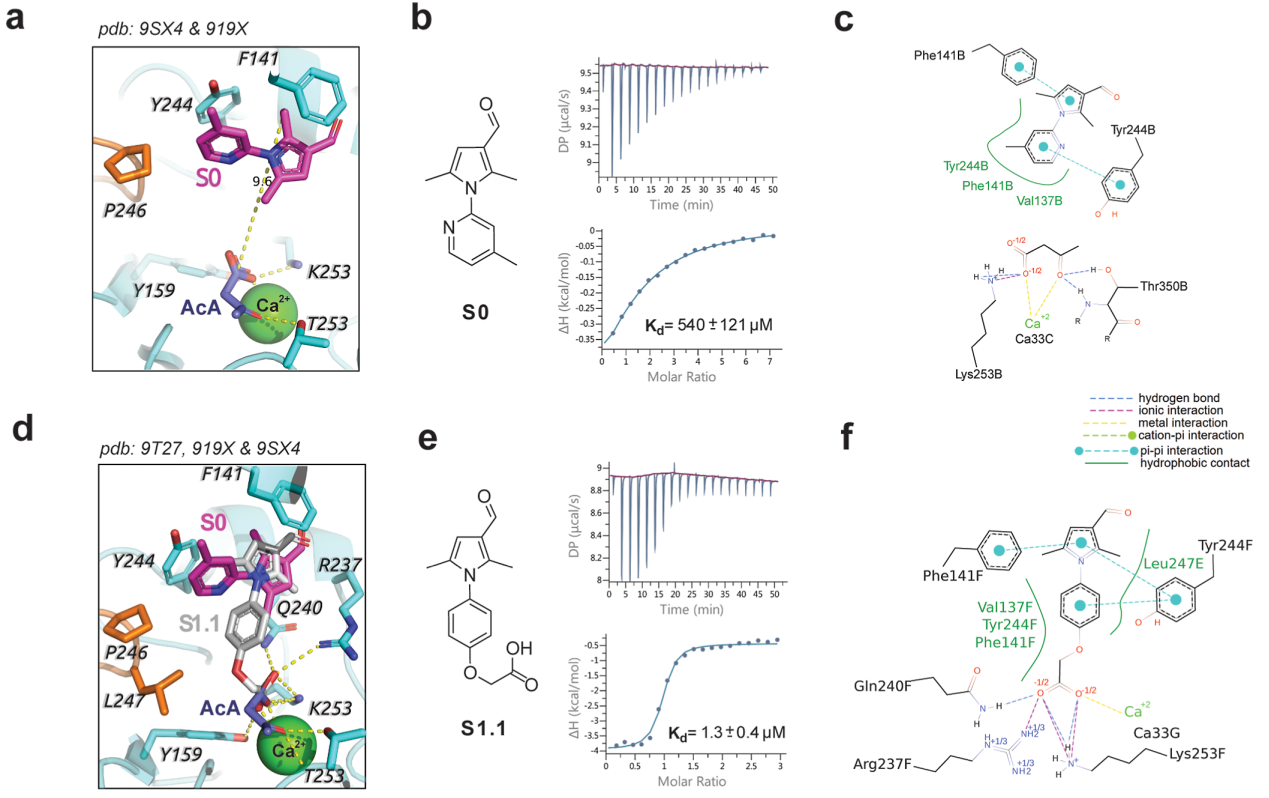
图3. 初始片段S0与先导化合物 S1.1 的结合位点、ITC 热谱及分子相互作用模式
化学骨架拓展与成药性改造
为拓展化学多样性,团队以S1.1复合物构建药效团模型,筛选获得结构全新的磺酰胺类化合物;其中S2.1及其衍生物亲和力达1–2 μM,并能与二聚界面形成CH-π相互作用。然而含羧酸化合物因为其亲水性过强,细胞膜穿透性差,所以团队将羧酸替换为四氮唑,获得的S3系列在保持低微摩尔级亲和力的同时显著改善了脂溶性与细胞通透性。
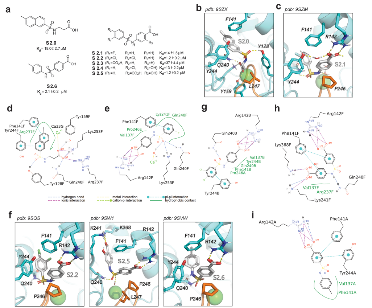
图4. 磺酰胺类S2系列化合物结构、晶体结合位点及分子相互作用图谱
药理学伴侣功能验证
DOSY-NMR显示候选化合物能促使G337S突变体从无活性的单体向活性二聚体转变;圆二色谱检测进一步证实,化合物能显著抑制突变蛋白解折叠与聚集,在数小时内维持二级结构稳定。
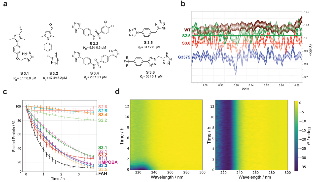
图5. 四氮唑类S3系列化合物结构、DOSY-NMR蛋白扩散实验、圆二色谱蛋白稳定性动力学
酶活测试显示,适量S2.5可使G337S-FAH的底物转化率提升约30%,但过高浓度会因占据活性口袋而产生抑制,呈现剂量依赖性的双向调节。
最后,在CRISPR编辑的HEK293T-G337S细胞模型中,发现S3.6处理16小时即带来FAH蛋白水平的剂量依赖性回升;而在G337S基因敲入小鼠中,单次腹腔注射S3.1和S3.3后3小时,肝脏Western Blot显示FAH蛋白水平分别恢复约4倍和5倍,初步证实了这类药理学伴侣在体内的蛋白稳定效应与治疗潜力。
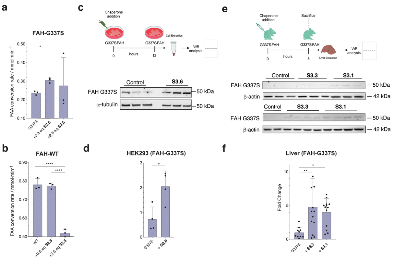
图6. 药理学伴侣对G337S-FAH 酶活性、细胞模型及小鼠肝组织蛋白水平的调控作用
总结
本研究依托人源FAH高分辨率晶体结构,开展了基于结构的理性药物设计,成功研发出可稳定G337S突变型FAH蛋白的小分子药理学伴侣。该类化合物可以促进突变蛋白由单体向活性二聚体转变,抑制蛋白解折叠与聚集,动物实验表明其具有显著的功能恢复效果。
相较于临床现有药物尼替西农仅阻断代谢通路、无法修复FAH蛋白缺陷的短板,本研究开发的小分子药理学伴侣直击HT1的发病分子机制,可以从蛋白稳态层面恢复FAH 酶功能。既为HT1提供了全新精准治疗靶点与候选先导化合物,也为蛋白错误折叠类疾病的治疗提供了完整的结构导向药物发现范式,具有重要的基础研究价值与临床转化前景。




















