01 成果简介
2025年7月24日,美国弗雷德里克国家癌症研究实验室Frank McCormick、Dhirendra K. Simanshu、日本第一三共株式会社Jun Tanaka、Kazuishi Kubota等研究人员在Science上发表了题为“Molecular glues that facilitate RAS binding to PI3Kα promote glucose uptake without insulin”的文章。
该研究发现了一种名为D223和D927的分子胶,它们能够显著增强RAS蛋白与PI3Kα催化亚基p110α的结合,从而促进葡萄糖摄取,且这一过程不依赖于胰岛素。这一发现为糖尿病治疗提供了新的思路。
研究人员通过化学蛋白质组学、结构生物学和动物模型实验,揭示了这些分子胶的作用机制,并验证了它们在改善糖尿病症状中的潜在应用价值。
02 背景介绍
糖尿病的发病机制与胰岛素信号传导缺陷密切相关。胰岛素通过激活PI3Kα-AKT信号通路,促进葡萄糖转运蛋白4(GLUT4)的转运,从而促进葡萄糖摄取。然而,在糖尿病患者中,胰岛素信号通路的功能受损,会导致胰岛素抵抗或胰岛素分泌不足。PI3Kα在胰岛素信号传导中起着核心作用,其催化亚单位p110α的激活突变与多种疾病相关。因此,寻找能够激活PI3Kα通路的新型分子,以模拟胰岛素的作用并改善糖尿病患者的血糖控制,是当前糖尿病治疗研究的重要方向。
03 图文概览
化合物的发现与初步验证
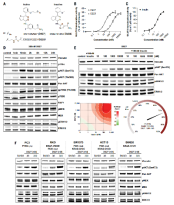
图1. D223和D927对GLUT4转运和PI3Kα信号通路的影响
实验结果表明, D223和D927能够模拟胰岛素的作用,选择性激活PI3Kα-AKT通路来促进葡萄糖摄取。
分子胶的作用机制和结构基础
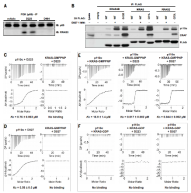
图2. D927增强RAS蛋白与p110α的结合亲和力

图3. D223和D927增强RAS与p110α结合的结构基础
通过免疫共沉淀和等温滴定量热法,揭示了D927作为一种分子胶,能够直接与p110α结合,并招募活性RAS蛋白,从而激活PI3Kα通路。
通过X射线晶体学解析了D223和D927与PI3Kα的RAS结合域(RBD)的复合物结构,揭示了这些分子胶如何增强RAS与p110α的结合。这些结构信息揭示了分子胶的作用机制,并为药物设计提供了重要的结构基础。
RAS家族蛋白对PI3Kα激活的贡献
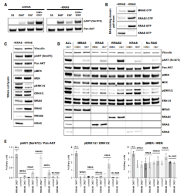
图4. D927对PI3Kα激活的RAS家族蛋白依赖性研究
基因敲除和细胞实验结果表明:D927通过增强RAS家族蛋白(尤其是RRAS2)与p110α的结合来激活PI3Kα信号通路,而不依赖于KRAS。
动物模型中的效果验证
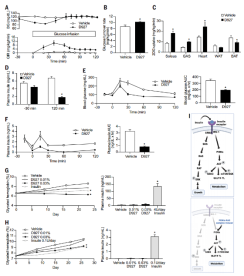
图5. D927在动物模型中的体内降糖效果
在动物模型中验证了分子胶的体内降糖效果及对糖尿病的改善作用,结果表明D927能够通过激活PI3Kα信号通路来改善糖尿病动物模型的血糖控制,且不依赖于胰岛素。这些发现进一步验证了D927作为潜在糖尿病治疗药物的潜力。
04 结果讨论
这项研究发现了一种新型的分子胶D223和D927,它们能够显著增强RAS蛋白与PI3Kα的结合亲和力,从而在没有胰岛素的情况下促进葡萄糖摄取。研究人员还通过X射线晶体学解析了D927和D223与PI3Kα的复合物结构,揭示了其增强RAS与PI3Kα结合的分子机制。
这些发现不仅为糖尿病治疗提供了新的潜在药物,还为理解PI3Kα-RAS相互作用的结构基础提供了重要信息,为发针对PI3Kα-RAS相互作用的癌症治疗药物提供了重要参考。




















